もうひとつの人体器官としての腸内マイクロバイオーム
人体にはさまざまな微生物が大量に存在しています。大部分はバクテリアですが、中にはウイルスや原虫、菌類、そして古細菌などもあります。これらは集合的にマイクロバイオームと言われています。腸内マイクロバイオータ、腸内フローラまたはマイクロバイオームとは、人間を含む動物の消化管に生息する微生物です。一部の細菌は疾患と関係していますが、その他の細菌は健康の多くの側面で特に重要な役割を果たしています。実際、人体には人間の細胞よりも多くの細菌細胞が存在しています。人間の細胞はわずか30兆個であるのに対し、細菌細胞は約40兆個に及びます。これら微生物の総重量は、脳とほぼ同じと言われています。微生物は、総体でもうひとつの人体器官として機能し、人間の健康に大きな役割を果たしています。腸内マイクロバイオームのゲノム全体では、体内のヒトDNAの量の100倍を超えています。その膨大な遺伝子学的潜在力を考えると、マイクロバイオータは人体の事実上すべての生理学的プロセスで何らかの役割を果たしていることが予想されます。腸内細菌はいくつかの精神疾患との関連が指摘されており、うつ病や双極性障害、統合失調症、自閉症など、さまざまな精神障害を抱える患者では、腸内微生物の組成が大きく変化していることがわかっています。
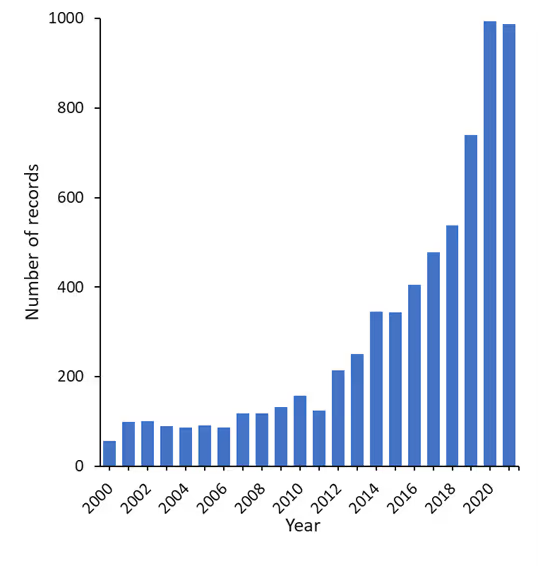
CAS コンテンツのコレクションTMの検索件数でわかるように、人間の健康、特にメンタルヘルスに関連する腸内マイクロバイオームへの関心は、2000年以降数年で指数関数的に増加しています。現在、メンタルヘルスと腸内マイクロバイオームに関する出版物は7,000以上あります(図1)。
新生児は出生時に最初の微生物を獲得。人間の腸内マイクロバイオームの発達
一般的には、子宮内は無菌環境であり、細菌定着は出生時に始まると考えられています。新生児のマイクロバイオームは分娩方法によって異なります。経膣分娩した新生児のマイクロバイオームは母体の膣内マイクロバイオームに似ており、帝王切開で出産した新生児のマイクロバイオームは母体の皮膚のマイクロバイオームに似ています。早産や授乳方法など、他のさまざまな要因が新生児のマイクロバイオームの発達に影響を及ぼします。成人期を通じた腸内マイクロバイオーム組成の主な決定要因は食事のようです。摂取する食事が変化すると、それに応じてマイクロバイオーム組成も急速に変化します。野菜中心の食事と肉食中心の食事では、それぞれ特徴的なパターンが見られます。腸内マイクロバイオームの発達と変化は、他の複数の要因によっても影響を受けます。CAS コンテンツのコレクションの検索によれば、ストレスにさらされることが、腸内マイクロバイオームの組成に影響を与える(食事に次いで)2番目に重要な要因になっています。その他の要因として、出産方法と乳児期の授乳方法、環境条件、投薬、ライフサイクルの段階と生活様式、併存疾患および医療処置などが挙げられます(図2)。その機能的組成および代謝活動の不均衡、または局所分布の変化によって引き起こされるマイクロバイオータの恒常性の崩壊は腸内毒素症と呼ばれ、微生物の不均衡または不適応を示しています。

現在認識されている腸内マイクロバイオームの組成に対する食事の役割の重要性、および腸内マイクロバイオームの健康への重大な影響を考慮すると、大きな疑問が残ります。腸内細菌を良好な状態に維持するために有益な、推奨される食事とは、どんなものなのでしょうか。特定の病気の治療法として特定の食品を挙げられるような明確な答えはありませんが、いくつかの主要なガイドラインが考案されています。食物繊維の多い食事は、腸内マイクロバイオータに特に影響を及ぼします。食物繊維は、結腸に生息するマイクロバイオータから生じる酵素でのみ消化および発酵が可能です。発酵により短鎖脂肪酸が放出され、結腸のpHが低下します。その非常に酸性の環境が、生き残る微生物マイクロバイオータの種類を決定します。pHが低くなると、クロストリジウム・ディフィシルなど、特定の有害な細菌の増殖が制限されます。イヌリン、でんぷん、ゴム質、ペクチン、フラクトオリゴ糖などの高繊維食品は、有益な微生物叢を養うため、プレバイオティクスとして知られるようになりました。こういったプレバイオティクス繊維は、一般的には果物や野菜、豆、そして小麦やオート麦、大麦などの全粒穀物に大量に含まれています。またそれとは別の非常に有益な食品類として、消化器系に良い生菌のプロバイオティクスがあります。これは、腸内マイクロバイオームをさらに改善させることがあります。これには、生きた活性培地を持つヨーグルトの一種であるケフィア、漬物、昆布茶、キムチ、味噌、ザワークラウトなどの発酵食品が含まれます。
腸内マイクロバイオータに属する菌種
人間の腸内マイクロバイオータは、門と呼ばれる多くのグループに分類されます。腸内マイクロバイオータは主に4つの門から成っています。フィルミクテス(Firmicutes)門、バクテロイデテス(Bacteroidetes)門、アクチノバクテリア(Actinobacteria)門、そしてプロテオバクテリア(Proteobacteria)門です。フィルミクテス門とバクテロイデテス門が腸内マイクロバイオータの90%を占めています。バクテリアの大部分は消化管内に存在し、ほとんどを占める嫌気性バクテリアは大腸に存在しています(図3)。

腸と脳の関係 - 「第2の脳」としての腸内マイクロバイオーム
腸と脳が常に双方向に対話をしていることは現在では確認されており、マイクロバイオータと代謝産物が主要な構成要素となっています。マイケル・ガーションは、1999年の著書で消化器系を「第2の脳」と呼びました。当時、科学者たちは人間の腸と脳が絶え間なく対話をしていること、そして腸の微生物が脳機能を大幅に調節していることに気づき始めていました。
現在では、腸内マイクロバイオータが、神経や内分泌経路そして免疫経路を介して中枢神経系と対話し、それにより脳機能を制御しているということが一般的に考えられています。さまざまな研究でも、腸内マイクロバイオータは、不安や気分、認知そして痛みの制御において大きな役割を果たしていることが示されています。したがって、マイクロバイオータ・腸・脳の関係という新たな概念は、腸内マイクロバイオータの調節機能が中枢神経系障害の新しい治療法を開発する、効果的な戦略となる可能性があることを示唆しています。
腸内マイクロバイオータとCOVID-19
最近、腸内マイクロバイオータの組成と、COVID-19患者のサイトカインおよび炎症マーカーのレベルとの間に相関関係が報告されています。腸内マイクロバイオームは、宿主の免疫応答を調節することにより、COVID-19の重症度に関与していることが示唆されています。さらに、腸内マイクロバイオームによる腸内毒素症は、病気から回復した後も症状が持続する要因となる可能性があり、腸内細菌が炎症とCOVID-19にどう関与しているかを理解する必要があることを強調しています。
腸内微生物の神経活性代謝物
腸内マイクロバイオータ・脳の関係の異常が、神経疾患の病態生理学における重大な要因として出現してきたため、腸内細菌代謝物の神経活性の可能性を理解するべく、ますます多くの研究が行われています。従って、主要な神経活性腸内微生物代謝物は次のように現れています。
神経伝達物質
腸内マイクロバイオームは、脳の活動を調節する神経伝達物質を生成します。中枢神経系の神経伝達物質の大部分は消化管にも存在し、腸の運動、分泌、細胞シグナル伝達の調節などの局所的な効果を発揮します。腸内マイクロバイオータの構成要素は神経伝達物質を合成することができます。例えば、乳酸桿菌とビフィズス菌はGABAを生成し、大腸菌はセロトニンとドーパミンを、そして乳酸桿菌はアセチルコリンを生成します。(図4)信号は迷走神経を介して脳に送られます。

短鎖脂肪酸
短鎖脂肪酸は食物の炭水化物の嫌気性発酵により盲腸と結腸で生成される小さな有機化合物で、他のバクテリアに栄養を与え、大腸で容易に吸収されます。短鎖脂肪酸は、消化器系、免疫系、そして中枢神経系の機能に関与していますが、行動への影響についてはさまざまな見解があります。腸内マイクロバイオームによって最も多く生成される3種類の短鎖脂肪酸は、酢酸塩、酪酸塩、そしてプロピオン酸塩です(図5)。これらを投与したマウスでは。うつ病の症状が軽減されることが実証されています。食物繊維を発酵させ短鎖脂肪酸を生成するグラム陽性の嫌気性細菌は、フィーカリバクテリウムおよびコプロコッカスという細菌です。フィーカリバクテリウムは豊富に存在する腸内微生物であり、うつ病を含むさまざまな疾患に対して重要な免疫学的役割と臨床的関連性があります。

トリプトファン代謝物
トリプトファンはタンパク質の合成に関与する必須アミノ酸です。細菌酵素(トリプトファナーゼ)によるその代謝分解は、セロトニン、キヌレニン、インドールなどの気分調節特性を持つことが確認された神経活性分子を生じさせます(図6)。トリプトファンの食事による摂取は、ヒトの中枢神経系のセロトニン濃度を調節でき、トリプトファンが枯渇するとうつ病が悪化することがわかっています。

乳酸
乳酸(図6)は、主に乳酸菌(L. lactis、L. gasseri、L. reuteriなど)、ビフィズス菌、プロテオバクテリアによる食物繊維の発酵から発生する有機酸です。乳酸塩は、いくつかの細菌種によって短鎖脂肪酸に変換され、短鎖脂肪酸の蓄え全体に寄与します。乳酸は血流に吸収され、血液脳関門を通過できます。脳の中枢神経系のシグナル伝達における乳酸の役割は、よく知られています。グルタミン酸に代謝可能なため、エネルギー基質としてニューロンに使用されます。また、シナプス可塑性にも寄与し、記憶力の発達を引き起こします。
ビタミン
ラクトバチルス菌やビフィズス菌など、腸内のほとんどの細菌は、大腸での代謝の際にビタミン(特にビタミンB群とビタミンK群)を合成します。人のビタミン生産は、腸内マイクロバイオータに依存しています。ビタミンは、脳を含む人体のさまざまな生理学的プロセスにおいてあらゆる役割を担う重要な微量栄養素です。ビタミンは能動輸送により血液脳関門を越えて運ばれます。中枢神経系においては、ビタミンの役割はエネルギー恒常性から神経伝達物質産生にまで及びます。そのため、ビタミンが欠乏すると、神経機能に重大な悪影響が生じる場合があります。また、葉酸(ビタミンB9)は、うつ病の病状に広くかかわっているとされている微生物由来のビタミンです。
最近の革新的な治験中の治療法である糞便微生物移植は、現在臨床試験にて試験中で、治療上非常に有望であることがわかっています。過去5年間に、糞便移植に関連する約1,000件の文書がCAS コンテンツのコレクションに毎年追加されています。たとえば、糞便マイクロバイオータ移植は、抗生物質に反応しない再発性クロストリジウム・ディフィシルによって引き起こされる感染症の80〜90%を回復できることが報告されています。各種疾患の潜在的な治療法として、研究が増加している糞便マイクロバイオータ移植を使用した臨床試験が意味していることを、早急に研究する必要があります。
現在、消化器マイクロバイオータを介した脳・腸の軸の調節に関する研究が、最前線の画期的な新しい科学として脚光を浴びています。利用可能なデータの大部分は、ヒトへの効果に適用できないかもしれない基礎科学または動物モデルに基づいてています。したがって、栄養とライフスタイル医学の理想的なパーソナライズを実現するような、特定のプレバイオティクス化合物とプロバイオティクス株の個別処方が、依然として有望となっています。マイクロバイオームの機能および宿主と微生物の相互作用の根底にあるメカニズムの特徴をさらに解明するための継続的な取り組みにより、健康と病気におけるマイクロバイオームの役割に対する理解がいっそう進むでしょう。
新たなトレンドや新しいアプローチが、うつ病や不安神経症、PTSDに苦しむ何百万人もの人々をいかに助けているか、その詳細はサイケデリック薬とその治療法としての進歩に関するブログをご覧ください。